Molekularna struktura predstavlja precizan prostorni raspored atoma unutar molekule te sustav sila koji te atome drži na okupu. Razumijevanje ove strukture ključno je za razumijevanje fizikalnih i kemijskih svojstava tvari, od jednostavnih plinova do kompleksnih biopolimera poput DNA.
Priroda kemijskih veza: Temelj stabilnosti
Atomi se povezuju u molekule kako bi postigli niže energetsko stanje, najčešće popunjavanjem svojih valentnih ljuski elektronima. Glavni tipovi veza koji definiraju strukturu su:
- Kovalentna veza: Nastaje dijeljenjem elektronskih parova između atoma nemetala. Karakterizira je usmjerenost u prostoru, što izravno određuje oblik molekule.
- Ionska veza: Rezultat je elektrostatskog privlačenja između suprotno nabijenih iona. Iako se češće razmatra u kontekstu kristalnih rešetki, ključna je za stabilnost mnogih molekularnih spojeva.
- Metalna veza: Delokalizirani elektroni koji se slobodno kreću između pozitivnih jezgri, pružajući materijalu specifična svojstva poput vodljivosti.
Ključne fizikalne vrijednosti molekule
Svaku molekularnu strukturu definiraju mjerljive vrijednosti koje određuju njezin identitet i stabilnost:
- Duljina veze: Ravnotežna udaljenost između jezgri dvaju atoma. Određena je ravnotežom između privlačnih sila (jezgra-elektron) i odbojnih sila (jezgra-jezgra).
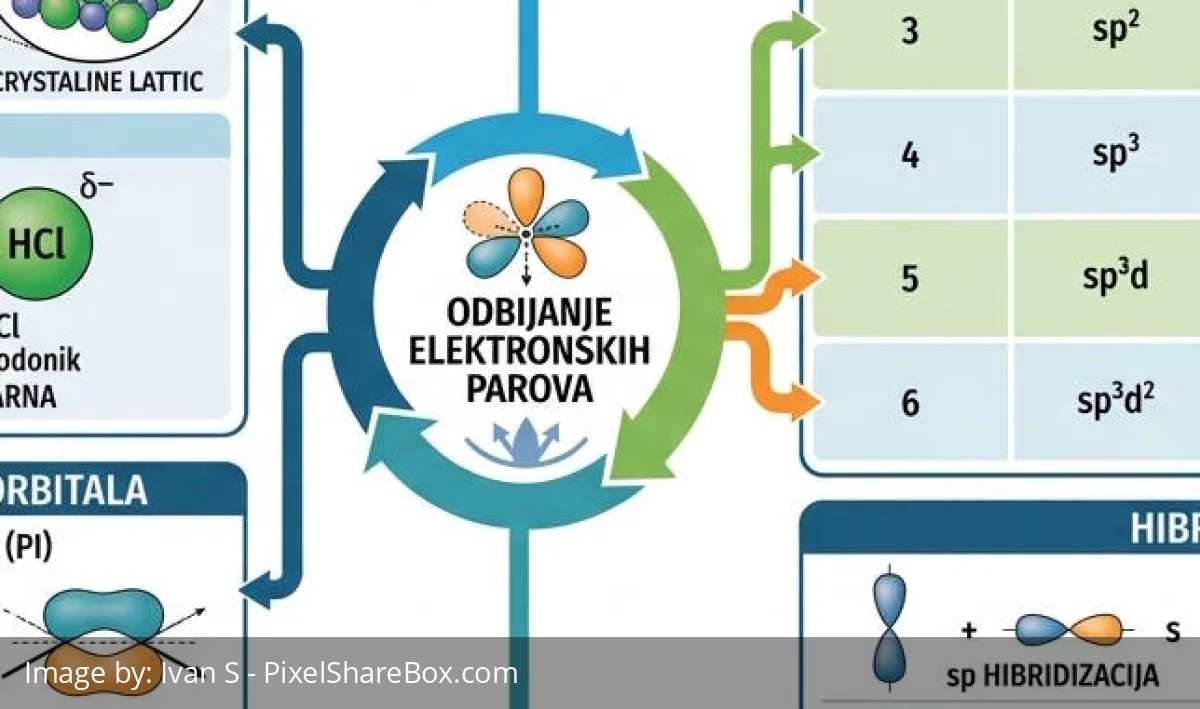
- Kut veze: Kut koji zatvaraju dvije kovalentne veze koje polaze iz istog centralnog atoma. Izračunava se pomoću VSEPR teorije (odbijanje elektronskih parova).
- Energija veze: Količina energije potrebna za kidanje veze. Veća energija podrazumijeva kraću i stabilniju vezu.
- Dipolni moment: Vektorska veličina koja opisuje raspodjelu električnog naboja, određujući je li molekula polarna ili nepolarna.
Dinamika veza: Kako se spajaju, raskidaju i mijenjaju?
Kemijska reaktivnost je proces kontinuirane transformacije veza:
- Spajanje (Sinteza): Kada se dva atoma približe na kritičnu udaljenost, njihove atomske orbitale se preklapaju, stvarajući molekularne orbitale. Sustav pritom oslobađa energiju (egzotermni proces).
- Raskidanje (Disocijacija): Za prekidanje veze potrebno je uložiti energiju (entalpija veze). To se može dogoditi homolitički (stvaranje radikala) ili heterolitički (stvaranje iona).
- Promjena (Rearanžman): Tijekom kemijskih reakcija, molekule prolaze kroz visokoenergetsko prijelazno stanje. U tom trenutku stare veze slabe, dok se nove počinju nazirati, što dovodi do rekonfiguracije cijele strukture.
Što čuva molekulu u njezinom obliku?
Stabilnost molekularnog oblika nije slučajna, već je rezultat strogo definiranih kvantnih i fizičkih čimbenika:
- Hibridizacija orbitala: Miješanje s, p i d orbitali (npr. sp3 hibridizacija kod ugljika) forsira atome da zauzmu točno određene geometrijske položaje (npr. tetraedar).
- Sterički efekti: Atomi i elektronski parovi zauzimaju prostor. “Sterička smetnja” sprječava dijelove molekule da se previše približe, čime se održava specifična konformacija.
- Međumolekulske sile: Vodikove veze i Van der Waalsove sile čuvaju sekundarne strukture kod velikih molekula (poput proteina), sprječavajući njihovo “raspadanje” u nefunkcionalne oblike.
Promjenjivost molekule
Molekula nije statičan entitet. Ona se neprestano mijenja kroz:
- Vibracije: Atomi titraju oko ravnotežnog položaja (osnova IC spektroskopije).
- Rotacije: Skupine atoma se mogu rotirati oko jednostrukih veza, mijenjajući konformaciju molekule.
- Izomerizaciju: Proces u kojem molekula zadržava isti broj atoma, ali mijenja njihov raspored, što potpuno mijenja njezinu biološku ili kemijsku funkciju.
Zaključak
Molekularna struktura je fascinantan spoj geometrijske preciznosti i energetske ravnoteže. Svaka veza, svaki kut i svaka vibracija unutar molekule rezultat su fundamentalnih sila prirode koje teže postizanju energetskog minimuma. Razumijevanje načina na koji se te veze formiraju i transformiraju omogućuje nam manipulaciju materijom na atomskoj razini — od stvaranja novih lijekova do razvoja naprednih materijala za budućnost.